

Leia com atenção todo este folheto antes de começar a utilizar ou a criança começar a utilizar este medicamento, pois contém informação importante para si ou para a sua criança.
• Conserve este folheto. Pode ter necessidade de o ler novamente.
• Caso ainda tenha dúvidas, fale com o seu médico ou enfermeiro.
• Esta vacina foi receitada apenas para si ou para a sua criança.
• Se tiver quaisquer efeitos indesejáveis, incluindo possíveis efeitos indesejáveis não indicados neste folheto, fale com o seu médico ou enfermeiro. Ver secção 4.
1. O que é BEXSERO e para que é utilizado
Bexsero é uma vacina contra o meningococo do grupo B.
Bexsero contém quatro componentes diferentes da superfície da bactéria Neisseria meningitidis do grupo B.
Bexsero é administrado a indivíduos a partir dos 2 meses de idade para auxiliar na proteção contra a doença provocada pela bactéria Neisseria meningitidis do grupo B. Estas bactérias podem causar infeções graves, e por vezes ameaçadoras da vida, como a meningite (inflamação das membranas que revestem o cérebro e a medula espinhal) e sépsis (infeção do sangue).
A vacina funciona através da estimulação específica do sistema de defesa natural do organismo da pessoa vacinada. Este processo resulta na proteção contra a doença.
2. O que precisa de saber antes de utilizar ou a sua criança utilizar BEXSERO
NÃO utilize Bexsero:
• se tem, ou se a sua criança tiver alergia às substâncias ativas ou a qualquer outro componente desta vacina (indicados na secção 6).
Advertências e precauções:
Fale com o seu médico ou enfermeiro antes de utilizar ou a sua criança utilizar Bexsero:
• se tiver ou se a criança tiver uma infeção grave com temperatura alta. Neste caso, a vacinação será adiada. A presença de uma infeção ligeira, por exemplo, uma constipação, não deverá exigir o adiamento da vacinação, mas fale primeiro com o seu médico ou enfermeiro.
• se tiver ou se a criança tiver hemofilia ou qualquer outro problema que possa impedir a coagulação correta do sangue, como o tratamento com medicamentos que tornam o sangue mais fluido (anticoagulantes). Fale primeiro com o seu médico ou enfermeiro.
• se estiver ou se a criança estiver a receber um tratamento que bloqueie a parte do sistema imunitário conhecida como ativação do complemento, tal como o eculizumab. Mesmo que tenha ou a criança tenha sido vacinada com Bexsero, permanece em risco aumentado de doença causada pela bactéria Neisseria meningitidis do grupo B.
• se a criança nasceu prematuramente (antes ou às 28 semanas de gestação), particularmente se tem dificuldades respiratórias. Paragens respiratórias ou respiração irregular durante um pequeno período de tempo podem ser mais frequentes nos primeiros três dias após a vacinação destes bebés, podendo necessitar de monitorização especial.
• se tiver ou a criança tiver uma alergia ao antibiótico canamicina. Se estiver presente, a quantidade de canamicina na vacina é baixa. Se tiver ou a sua criança tiver uma alergia à canamicina, fale primeiro com o seu médico ou enfermeiro.
Podem ocorrer reações como desmaio, sensação de desmaio ou outras reações relacionadas com o stress em resposta a qualquer injeção com agulha. Informe o seu médico ou enfermeiro se já tiver sofrido este tipo de reações anteriormente.
Não existem dados sobre a utilização de Bexsero em adultos com mais de 50 anos de idade. Existe informação limitada sobre a administração de Bexsero em doentes com condições médicas crónicas ou com um sistema imunitário enfraquecido. Se apresentar ou a sua criança apresentar um sistema imunitário enfraquecido (por exemplo, devido ao uso de medicamentos imunossupressores, ou infeção com VIH, ou defeitos hereditários no sistema de defesa natural do organismo), é possível que a eficácia de Bexsero seja reduzida.
Tal como com qualquer vacina, Bexsero poderá não proteger totalmente os indivíduos vacinados.
Outros medicamentos e Bexsero:
Informe o seu médico ou enfermeiro se estiver ou a sua criança estiver a tomar, tiverem tomado recentemente, ou se vierem a tomar outros medicamentos, ou se tiverem sido administradas recentemente qualquer outra vacina.
Bexsero pode ser administrado em simultâneo com qualquer um dos seguintes componentes de vacina: difteria, tétano, tosse convulsa (pertussis), Haemophilus influenzae tipo b, poliomielite, hepatite B, pneumococos, sarampo, papeira, rubéola, varicela e meningococo A, C, W, Y. Fale com o seu médico ou enfermeiro se precisar de mais informações.
Quando administrado ao mesmo tempo que outras vacinas, Bexsero deve ser administrado em locais de injeção distintos.
O seu médico ou enfermeiro poderão indicar-lhe que dê medicamentos à sua criança para baixar a febre no momento da injeção com Bexsero e após a injeção. Isto ajudará a reduzir alguns dos efeitos indesejáveis de Bexsero.
Gravidez e amamentação:
Se está grávida ou a amamentar, se pensa estar grávida ou planeia engravidar, consulte o seu médico antes de Bexsero lhe ser administrado. O seu médico poderá ainda assim recomendar a administração de Bexsero se estiver em risco de exposição a uma infeção meningocócica.
Condução de veículos e utilização de máquinas:
Os efeitos de Bexsero sobre a capacidade de conduzir e utilizar máquinas são nulos ou desprezáveis. No entanto, alguns dos efeitos mencionados na secção 4 “Efeitos indesejáveis possíveis poderão afetar temporariamente a capacidade de conduzir ou utilizar máquinas.
Bexsero contém cloreto de sódio:
Este medicamento contém menos de 1 mmol de sódio (23 mg) por dose, ou seja, é praticamente “isento de sódio.
3. Como utilizar BEXSERO
Bexsero (0,5 ml) será administrado à sua criança ou a si por um médico ou enfermeiro. Será injetado num músculo, normalmente na coxa dos lactentes ou no braço das crianças, adolescentes e adultos.
É importante seguir as instruções do médico ou enfermeiro para que cumpra, ou a sua criança cumpra o programa de injeções (doses).
Lactentes dos 2 meses aos 5 meses de idade, na altura da primeira dose:
Deverá ser administrado à sua criança um conjunto inicial de duas ou três doses (injeções) da vacina, seguidas de uma dose (injeção) adicional (reforço).
• A primeira dose (injeção) não deve ser administrada antes dos 2 meses de idade.
• Se forem administradas três doses iniciais, o intervalo entre as doses (injeções) deve ser de pelo menos 1 mês.
• Se forem administradas duas doses iniciais, o intervalo entre as doses (injeções) deve ser de pelo menos 2 meses.
• A dose de reforço será administrada entre os 12 e 15 meses de idade, após um intervalo de pelo menos 6 meses desde a última dose (injeção) do esquema inicial. Caso seja adiado, o reforço não deve ser administrado após os 24 meses de idade.
Lactentes dos 6 aos 11 meses de idade, na altura da primeira dose:
Deverão ser administradas aos lactentes entre os 6 e 11 meses de idade duas doses (injeções) da vacina, seguidas de uma dose (injeção) adicional (reforço).
• O intervalo entre cada injeção deve ser de pelo menos 2 meses.
• A dose de reforço será administrada no segundo ano de vida, após um intervalo de pelo menos 2 meses desde a segunda injeção.
Crianças dos 12 aos 23 meses de idade, na altura da primeira dose:
Deverão ser administradas às crianças entre os 12 e 23 meses de idade duas doses (injeções) da vacina, seguidas de uma dose (injeção) adicional (reforço).
• O intervalo entre cada injeção deve ser de pelo menos 2 meses.
• A dose de reforço será administrada após um intervalo de 12 a 23 meses desde a segunda injeção.
Crianças dos 2 aos 10 anos de idade, na altura da primeira dose:
Deverão ser administradas às crianças entre os 2 e 10 anos de idade duas doses (injeções) da vacina.
• O intervalo entre cada injeção deve ser de pelo menos 1 mês.
A sua criança poderá ter de administrar uma dose (injeção) adicional (reforço).
Adolescentes e adultos a partir dos 11 anos de idade, na altura da primeira dose:
Deverão ser administradas aos adolescentes (a partir dos 11 anos de idade) e adultos duas doses (injeções) da vacina.
• O intervalo entre cada injeção deve ser de pelo menos 1 mês. Poderá ter de administrar uma dose (injeção) adicional (reforço).
Adultos com mais de 50 anos de idade
Não existem dados em adultos com mais de 50 anos de idade. Fale com o seu médico para aconselhamento sobre se será benéfico para si administrar Bexsero.
Caso ainda tenha dúvidas acerca de Bexsero, fale com o seu médico ou enfermeiro.
4. Efeitos indesejáveis possíveis
Como todas as vacinas, esta vacina pode causar efeitos indesejáveis, embora estes não se manifestem em todas as pessoas.
Quando Bexsero for administrado a si ou à sua criança, os efeitos indesejáveis muito frequentes (podem ocorrer em mais de 1 em 10 pessoas) que poderá ter ou a sua criança poderá ter (notificados em todos os grupos etários) são:
• dor/sensibilidade no local de injeção, vermelhidão da pele no local de injeção, inchaço da pele no local de injeção, endurecimento da pele no local da injeção.
Os seguintes efeitos indesejáveis podem também ocorrer após a administração desta vacina.
Lactentes e crianças (até aos 10 anos de idade):
Muito frequentes (podem afetar mais de 1 em 10 pessoas): febre (≥ 38ºC), perda de apetite, sensibilidade no local de injeção (incluindo sensibilidade grave no local de injeção, demonstrada ao chorar quando o membro injetado é manipulado/mexido), dor nas articulações, erupção na pele (crianças entre os 12 e 23 meses de idade) (pouco frequente após a dose de reforço), sonolência, irritabilidade, choro invulgar, vómitos (pouco frequente após a dose de reforço), diarreia,dor de cabeça.
Frequentes (podem afetar até 1 em 10 pessoas): erupção na pele (lactentes e crianças entre os 2 e 10 anos de idade).
Pouco frequentes (podem afetar até 1 em 100 pessoas): febre alta (≥ 40°C), convulsões (incluindo convulsões febris), pele seca, palidez (raro após a dose de reforço).
Raros (podem afetar até 1 em 1.000 pessoas): doença de Kawasaki, podendo incluir sintomas como febre com duração superior a cinco dias, associada a erupção na pele (manchas na pele) no tronco, por vezes seguida de descamação da pele das mãos e dedos, gânglios inchados no pescoço e olhos, lábios, garganta e língua vermelhos, erupção na pele com ou sem comichão.
Adolescentes (a partir dos 11 anos de idade) e adultos:
Muito frequentes (podem afetar mais de 1 em 10 pessoas): dor no local de injeção com incapacidade de realizar a atividade normal do dia-a-dia, dores nos músculos e articulações, náuseas, sensação de mal-estar geral, dor de cabeça.
Os efeitos indesejáveis notificados após a introdução no mercado incluem: Gânglios linfáticos aumentados de volume.
Reações alérgicas que podem incluir inchaço grave dos lábios, boca, garganta (podendo causar dificuldades ao engolir), dificuldades respiratórias com pieira ou tosse, erupção na pele, perda de consciência e tensão arterial muito baixa.
Colapso (início súbito de fraqueza muscular), menos respondedor(a) que o habitual ou falta de consciência e palidez ou coloração azulada da pele em crianças pequenas.
Sensação de desmaio ou desmaio.
Erupção na pele (adolescentes a partir dos 11 anos de idade e adultos). Febre (adolescentes a partir dos 11 anos de idade e adultos).
Reações no local de injeção como inchaço extenso do membro vacinado, bolhas no local de injeção ou em redor do mesmo e nódulo duro no local de injeção (que pode persistir por mais de um mês).
Foram notificadas esporadicamente pouco tempo após a vacinação rigidez do pescoço ou sensação de desconforto à luz (fotofobia), indicando irritação meníngea. Estes sintomas foram de natureza ligeira e transitória.
Comunicação de efeitos indesejáveis:
Se tiver quaisquer efeitos indesejáveis, incluindo possíveis efeitos indesejáveis não indicados neste folheto, fale com o seu médico, farmacêutico ou enfermeiro. Também poderá comunicar efeitos indesejáveis diretamente através do sistema nacional de notificação mencionado no Apêndice V. Ao comunicar efeitos indesejáveis, estará a ajudar a fornecer mais informações sobre a segurança deste medicamento.
5. Como conservar BEXSERO
Manter esta vacina fora da vista e do alcance das crianças.
Não utilize esta vacina após o prazo de validade impresso na embalagem e no rótulo da seringa pré- cheia após EXP. O prazo de validade corresponde ao último dia do mês indicado.
Conservar no frigorífico (2°C – 8°C). Não congelar. Conservar na embalagem de origem para proteger da luz.
Não deite fora quaisquer medicamentos na canalização ou no lixo doméstico. Pergunte ao seu médico ou enfermeiro como deitar fora os medicamentos que já não utiliza. Estas medidas ajudarão a proteger o ambiente.
6. Conteúdo da embalagem e outras informações
Qual a composição de Bexsero:
Uma dose (0,5 ml) contém:
Substâncias ativas:
Proteína de fusão NHBA recombinante de Neisseria meningitidis do grupo B(1, 2, 3): 50 microgramas Proteína NadA recombinante de Neisseria meningitidis do grupo B(1, 2, 3): 50 microgramas Proteína de fusão fHbp recombinante de Neisseria meningitidis do grupo B(1, 2, 3): 50 microgramas
Vesículas de membrana externa (VME) de Neisseria meningitidis do grupo B estirpe NZ98/254, medidas como a quantidade de proteína total com PorA P1.4 2: 25 microgramas
(1) produzida em células de E. coli por tecnologia de ADN recombinante
(2) adsorvida em hidróxido de alumínio (0,5 mg de Al3+)
(3) NHBA (Antigénio de Neisseria de Ligação à Heparina), NadA (Adesina A de Neisseria), fHbp (proteína ligante de fator H)
Outros componentes:
Cloreto de sódio, histidina, sacarose e água para preparações injetáveis (ver secção 2 para mais informações sobre sódio).
Qual o aspeto de Bexsero e conteúdo da embalagem:
Bexsero é uma suspensão branca opalescente.
Bexsero está disponível em 1 dose em seringa pré-cheia com ou sem agulhas separadas, embalagens de 1 e 10.
É possível que não sejam comercializadas todas as apresentações.
Titular da Autorização de Introdução no Mercado:
GSK Vaccines S.r.l.
Via Fiorentina 1
53100 Siena
Itália
Fabricante:
GSK Vaccines S.r.l.
Bellaria-Rosia
53018 Sovicille (Siena)
Itália
Para quaisquer informações sobre este medicamento, queira contactar o representante local do Titular da Autorização de Introdução no Mercado:
België/Belgique/Belgien
GlaxoSmithKline Pharmaceuticals SA/NV
Tél/Tel: + 32 10 85 52 00
Lietuva
GSK Vaccines S.r.l.
Tel: +370 80000334
България
GSK Vaccines S.r.l.
Тел. +359 80018205
Luxembourg/Luxemburg
GlaxoSmithKline Pharmaceuticals SA/NV
Tél/Tel: + 32 10 85 52 00
Česká republika
GlaxoSmithKline s.r.o.
Tel: + 420 2 22 00 11 11
cz.info@gsk.com
Magyarország
GSK Vaccines S.r.l.
Tel.: +36 80088309
Danmark
GlaxoSmithKline Pharma A/S
Tlf: + 45 36 35 91 00
dk-info@gsk.com
Malta
GSK Vaccines S.r.l.
Tel: +356 80065004
Deutschland
GlaxoSmithKline GmbH & Co. KG
Tel: +49 (0)89 36044 8701
de.impfservice@gsk.com
Eesti
GSK Vaccines S.r.l.
Tel: +372 8002640
Nederland
GlaxoSmithKline BV
Tel: + 31 (0)33 2081100
Norge
GlaxoSmithKline AS
Tlf: + 47 22 70 20 00
Ελλάδα
GlaxoSmithKline Μονοπρόσωπη A.E.B.E
Tηλ: + 30 210 68 82 100
Österreich
GlaxoSmithKline Pharma GmbH
Tel: + 43 (0)1 97075 0
at.info@gsk.com
España GlaxoSmithKline, S.A.
Tel: + 34 900 202 700
es-ci@gsk.com
Polska
GSK Services Sp. z o.o.
Tel.: + 48 (22) 576 9000
France
Laboratoire GlaxoSmithKline
Tél: + 33 (0) 1 39 17 84 44
diam@gsk.com
Portugal
GlaxoSmithKline - Produtos Farmacêuticos, Lda.
Tel: + 351 21 412 95 00
FI.PT@gsk.com
Hrvatska
GSK Vaccines S.r.l.
România
GSK Vaccines S.r.l.
Tel.: +385 800787089
Tel: +40 800672524
Ireland
GlaxoSmithKline (Ireland) Ltd
Tel: + 353 (0)1 495 5000
Slovenija
GSK Vaccines S.r.l.
Tel: +386 80688869
Ísland
Vistor hf.
Sími: +354 535 7000
Slovenská republika
GSK Vaccines S.r.l.
Tel.: +421 800500589
Italia
GlaxoSmithKline S.p.A.
Tel: +39 (0)45 7741 111
Suomi/Finland
GlaxoSmithKline Oy
Puh/Tel: + 358 10 30 30 30
Κύπρος
GSK Vaccines S.r.l.
Τηλ: +357 80070017
Sverige
GlaxoSmithKline AB
Tel: + 46 (0)8 638 93 00
info.produkt@gsk.com
Latvija
GSK Vaccines S.r.l.
Tel: +371 80205045
United Kingdom (Northern Ireland)
GSK Vaccines S.r.l.
Tel: +44 (0)800 221 441
customercontactuk@gsk.com
Está disponível informação pormenorizada sobre este medicamento no sítio da internet da Agência Europeia de Medicamentos: http://www.ema.europa.eu.
7. Outra informação
A informação que se segue destina-se apenas aos profissionais de saúde:
Durante o armazenamento, pode observar-se um depósito esbranquiçado fino na seringa pré-cheia contendo a suspensão.
Antes da utilização, a vacina deve ser bem agitada para formar uma suspensão homogénea.
A vacina deve ser examinada visualmente para detetar partículas e descoloração antes da administração. Em caso de presença de partículas estranhas e/ou alteração do aspeto físico, a vacina não deve ser administrada. Se forem fornecidas duas agulhas de comprimentos diferentes na embalagem, escolha a agulha adequada para assegurar uma administração intramuscular.
Não congelar.
Bexsero não deve ser misturado com outras vacinas na mesma seringa.
Se for necessária a administração concomitante de outras vacinas, as vacinas devem ser administradas em locais de injeção distintos.
Deve assegurar-se que a vacina é injetada apenas por via intramuscular.
Instruções para a seringa pré-cheia:
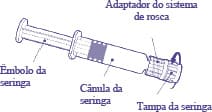
Segure a seringa pela cânula e não pelo êmbolo da seringa.
Desenrosque a tampa da seringa rodando-a no sentido contrário dos ponteiros do relógio.
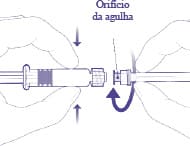
Para colocar a agulha na seringa, ligue o orifício da agulha ao adaptador do sistema de rosca, rodando um quarto de volta no sentido dos ponteiros do relógio até sentir que está fixo.
Não puxe o êmbolo da seringa para fora da cânula da seringa. Se isso acontecer, não administre a vacina.
Eliminação:
Qualquer medicamento não utilizado ou resíduos devem ser eliminados de acordo com as exigências locais.













