Leia com atenção todo este folheto antes de começar a utilizar este medicamento pois contém informação importante para si.
• Conserve este folheto. Pode ter necessidade de o ler novamente.
• Caso ainda tenha dúvidas, fale com o seu médico, farmacêutico ou enfermeiro.
• Este medicamento foi receitado apenas para si. Não deve dá-lo a outros. O medicamento pode ser-lhes prejudicial mesmo que apresentem os mesmos sinais de doença.
• Se tiver quaisquer efeitos indesejáveis, incluindo possíveis efeitos indesejáveis não indicados neste folheto, fale com o seu médico, farmacêutico ou enfermeiro. Ver secção 4.
1. O que é ELIGARD e para que é utilizado
A substância ativa do ELIGARD pertence ao grupo das hormonas libertadoras da gonadotropina. Estes medicamentos são utilizados para diminuir a produção de determinadas hormonas sexuais (testosterona).
ELIGARD é utilizado para o tratamento do cancro da próstata metastático hormonodependente em homens adultos e para o tratamento do cancro da próstata não metastático hormonodependente de alto risco em combinação com radioterapia.
2. O que precisa de saber antes de utilizar ELIGARD
Não utilize ELIGARD
• Se é mulher ou criança.
• Se tem hipersensibilidade (alergia) à substância ativa acetato de leuprorrelina, a medicamentos com atividade comparável à da hormona gonadotropina que existe naturalmente ou a qualquer outro componente do ELIGARD (indicados na secção 6).
• Após remoção cirúrgica dos testículos, sendo que nesse caso o ELIGARD não conduz a uma diminuição adicional dos níveis séricos de testosterona.
• Como único tratamento se tem sintomas relacionados com pressão na medula espinal ou tumor na coluna espinal. Neste caso, o ELIGARD pode apenas ser utilizado em combinação com outros medicamentos para o cancro da próstata.
Advertências e precauções:
Fale com o seu médico, farmacêutico ou enfermeiro antes de utilizar ELIGARD:
• Se tiver qualquer uma das seguintes situações: qualquer condição cardíaca ou dos vasos sanguíneos, incluindo problemas de ritmo cardíaco (arritmia), ou está a ser tratado com medicamentos para estas situações. O risco de problemas de ritmo cardíaco pode ser aumentado quando se utiliza ELIGARD.
• Se tiver dificuldades em urinar. Deverá ser monitorizado atentamente durante as primeiras semanas do tratamento.
• Se surgir pressão na medula espinal ou dificuldades em urinar. Em relação a outros medicamentos que têm um mecanismo de ação semelhante ao do ELIGARD, foi comunicado que casos graves de pressão na medula espinal e estreitamento dos tubos entre os rins e a bexiga podem contribuir para sintomas típicos de paralisia. Se surgirem estas complicações deve ser iniciada uma terapia padrão.
• Se sentir dores de cabeça repentinas, vómitos, um estado mental alterado, e por vezes colapso cardiovascular, após 2 semanas a tomar ELIGARD, alerte o seu médico ou profissionais de saúde. Estes são casos raros denominados como apoplexia pituitária, que foram comunicados COM OUTROS MEDICAMENTOS que têm um mecanismo de ação similar ao do ELIGARD.
• Se sofre de diabetes mellitus (níveis elevados de açúcar no sangue). Deverá ser monitorizado regularmente durante o tratamento.
• O tratamento com ELIGARD pode aumentar o risco de fraturas devido a osteoporose (diminuição da densidade óssea).
• Foram comunicados casos de depressão em doentes que tomam ELIGARD. Se estiver a tomar ELIGARD e desenvolver um humor deprimido, informe o seu médico.
• Foram comunicados acontecimentos cardiovasculares em doentes que utilizam medicamentos similares ao ELIGARD, mas desconhece-se a sua relação com estes medicamentos. Se estiver a tomar ELIGARD e desenvolver sinais ou sintomas cardiovasculares, informe o seu médico.
• Foram comunicadas convulsões em doentes após administração de ELIGARD. Se estiver a tomar ELIGARD e desenvolver convulsões, informe o seu médico.
• Se sofrer de uma dor de cabeça má ou recorrente, problemas com a visão e tinido ou zunido nos ouvidos, contacte imediatamente o seu médico.
• Se tem fígado gordo
Foram notificados efeitos indesejáveis cutâneos graves, incluindo síndrome de Stevens- Johnson (SJS) e Necrólise epidérmica tóxica (NET), em associação com a leuprorrelina. Pare de utilizar leuprorrelina e consulte imediatamente um médico se tiver qualquer um dos sintomas relacionados com estas reações cutâneas graves descritas na seção 4.
Complicações iniciais do tratamento:
Durante a primeira semana de tratamento, há geralmente um ligeiro aumento da hormona sexual masculina, testosterona, no sangue. Isto pode levar a uma deterioração temporária dos sintomas relacionados com a doença e também à ocorrência de novos sintomas que não foram sentidos até esse ponto. Estes incluem especialmente dor óssea, perturbações urinárias, pressão na medula espinal, ou a secreção de sangue na urina. Estes sintomas geralmente diminuem com a continuação do tratamento. Se os sintomas não diminuírem, deverá contactar o seu médico.
Se ELIGARD não ajudar:
Uma proporção dos doentes terá tumores que não são sensíveis à diminuição dos níveis séricos de testosterona. Fale com o seu médico se tiver a impressão de que o efeito do ELIGARD é demasiado fraco.
Outros medicamentos e ELIGARD:
ELIGARD pode interferir com alguns medicamentos usados para tratar problemas de ritmo cardíaco (por exemplo, quinidina, procainamida, amiodarona e sotalol) ou pode aumentar o risco de problemas de ritmo cardíaco quando utilizado com outros medicamentos (por exemplo, a metadona (utilizado para o alívio da dor e para desintoxicação por dependência de drogas), moxifloxacina (um antibiótico), antipsicóticos usados para doenças mentais graves).
Informe o seu médico ou farmacêutico se estiver a tomar ou tiver tomado recentemente outros medicamentos, incluindo medicamentos obtidos sem receita médica.
Gravidez e amamentação:
O ELIGARD não se destina a mulheres.
Condução de veículos e utilização de máquinas:
A fadiga, tonturas e perturbações visuais são efeitos indesejáveis possíveis do tratamento com o ELIGARD ou podem ser resultantes da doença subjacente. Se sofrer estes efeitos indesejáveis, deverá ter cuidado ao conduzir e utilizar máquinas.
3. Como utilizar ELIGARD
Dosagem:
Utilize sempre este medicamento exatamente como indicado pelo seu médico ou farmacêutico. Fale com o seu médico ou farmacêutico se tiver dúvidas.
Se não for prescrito de outra forma pelo médico, ELIGARD 22,5 mg é administrado uma vez de três em três meses.
A solução injetada forma um depósito da substância ativa a partir do qual ocorre uma libertação contínua da substância ativa, acetato de leuprorrelina, por um período de três meses.
Testes adicionais:
A resposta à terapia com ELIGARD deve ser verificada pelo seu médico por intermédio da verificação de valores clínicos específicos e pela medição do nível sérico do chamado antigénio específico da próstata (PSA).
Modo de administração:
O ELIGARD deverá apenas ser administrado pelo seu médico ou enfermeiro, os quais estarão também encarregues da preparação do mesmo.
Após a preparação, ELIGARD é administrado por injeção subcutânea (injeção no tecido abaixo da pele). A injeção intra-arterial (numa artéria) ou intravenosa (numa veia) necessita ser estritamente evitada. Tal como para outras substâncias ativas que são injetadas subcutaneamente, o local da injeção deve variar periodicamente.
Se administrar mais ELIGARD do que deveria:
Uma vez que a injeção é geralmente administrada pelo seu médico ou pessoal devidamente qualificado, não é esperada sobredosagem.
Se uma quantidade maior que a pretendida for administrada, o seu médico irá monitorizá-lo cuidadosamente e dar-lhe-á tratamento adicional conforme necessário.
Caso se tenha esquecido de administrar ELIGARD:
Por favor, fale com o seu médico se acredita que a sua administração trimestral de ELIGARD foi esquecida.
Efeitos quando o tratamento com ELIGARD é interrompido:
Como regra geral, a terapia do cancro da próstata com ELIGARD requer um tratamento de longa duração. Consequentemente, a terapêutica não deve ser interrompida, mesmo que existam melhorias nos sintomas ou que estes desapareçam completamente.
Se o tratamento com ELIGARD for interrompido prematuramente, pode ocorrer a deterioração dos sintomas relacionados com a doença.
Não deverá interromper a terapêutica prematuramente sem consultar previamente o seu médico.
Se tiver qualquer dúvida adicional acerca da utilização deste medicamento, consulte o seu médico, farmacêutico ou enfermeiro.
4. Efeitos indesejáveis possíveis
Como todos os medicamentos, o ELIGARD pode causar efeitos indesejáveis, no entanto estes não se manifestam em todas as pessoas.
Os efeitos indesejáveis que foram observados durante o tratamento com ELIGARD são principalmente atribuídos ao efeito específico da substância ativa acetato de leuprorrelina, nomeadamente o aumento e a diminuição de certas hormonas. Os efeitos indesejáveis descritos mais frequentemente são os afrontamentos (aproximadamente 58% dos doentes), náuseas, mal- estar e a fadiga, assim como irritações locais temporárias no local da injeção.
Efeitos indesejáveis iniciais:
Durante as primeiras semanas do tratamento com ELIGARD, pode ocorrer o agravamento de sintomas específicos da doença, uma vez que numa primeira fase existe geralmente um breve aumento da testosterona sanguínea, hormona sexual masculina. Consequentemente, o seu médico pode administrar um antiandrogénio apropriado (substância que inibe o efeito da
testosterona) na fase inicial do tratamento de modo a reduzir estes possíveis efeitos indesejáveis (Ver também a Secção 2 Antes de utilizar o ELIGARD, Complicações Iniciais do Tratamento).
Efeitos indesejáveis locais:
Os efeitos indesejáveis locais que têm sido descritos após a injeção do ELIGARD são tipicamente consistentes com os que são frequentemente associados a preparações similares injetadas subcutaneamente (preparações que são injetadas nos tecidos por baixo da pele). O ardor ligeiro imediatamente após a injeção é muito frequente. A picada e a dor após a injeção são frequentes, assim como um hematoma no local da injeção. A vermelhidão da pele no local da injeção foi notificada como um acontecimento frequente. O endurecimento dos tecidos e ulceração são pouco frequentes.
Estes efeitos indesejáveis localizados após injeção subcutânea são ligeiros e descritos como sendo de breve duração. Eles não ocorrem novamente entre as injeções individuais.
Efeitos indesejáveis muito frequentes (podem afetar mais de 1 em cada 10 doentes):
◦ Afrontamentos
◦ Hemorragias espontâneas na pele ou nas membranas mucosas, vermelhidão da pele
◦ Fadiga, efeitos indesejáveis relacionados com a injeção (ver também acima efeitos indesejáveis locais)
Efeitos indesejáveis frequentes (podem afetar até 1 em cada 10 doentes):
◦ Nasofaringite (sintomas da constipação comum)
◦ Náusea, mal-estar, diarreia, inflamação do estômago e intestinos (gastroenterite/colite)
◦ Comichão, suores noturnos
◦ Dor nas articulações
◦ Idas irregulares à casa de banho para urinar (também durante a noite), dificuldade no início da micção, micção dolorosa, quantidade de urina reduzida.
◦ Sensibilidade mamária, hipertrofia mamária, atrofia testicular, dor testicular, infertilidade, disfunção eréctil, redução do tamanho do pénis
◦ Rigidez (episódios de tremores exagerados com febres elevadas), fraqueza
◦ Tempo de hemorragia prolongado, alterações hematológicas, diminuição dos glóbulos vermelhos/baixa contagem de glóbulos vermelhos
Efeitos indesejáveis pouco frequentes (podem afetar até 1 em cada 100 doentes):
◦ Infeção do trato urinário, infeção local da pele
◦ Agravamento da diabetes mellitus
◦ Sonhos anormais, depressão, diminuição da libido
◦ Tonturas, dores de cabeça, alterações da sensibilidade da pele, insónia, distúrbios do gosto, distúrbios do olfato
◦ Hipertensão (aumento da pressão sanguínea), hipotensão (diminuição da pressão sanguínea)
◦ Dificuldade em respirar
◦ Prisão de ventre, boca seca, dispepsia (perturbações na digestão, com sintomas de estômago cheio, dor no estômago, arrotos, náusea, vómitos, sensação de ardor no estômago), vómitos
◦ Humidade, aumento da sudação
◦ Dores nas costas, cãibras musculares
◦ Hematúria (sangue na urina)
◦ Espasmos na bexiga, mais idas à casa de banho, para urinar, do que o normal, incapacidade para urinar
◦ Aumento do tecido mamário no homem, impotência
◦ Letargia (sonolência), dor, febre
◦ Aumento de peso
◦ Perda de equilíbrio, atordoamento
◦ Perda muscular/perda de tecido muscular após utilização prolongada
Efeitos indesejáveis raros (podem afetar até 1 em cada 1 000 doentes):
◦ Movimentos involuntários anormais
◦ Perda súbita da consciência e desmaio
◦ Flatulência, arrotos
◦ Perda de cabelo, erupções na pele (borbulhas na pele)
◦ Dor mamária
◦ Ulceração no local de injeção
Efeitos indesejáveis muito raros (podem afetar até 1 em cada 10 000 doentes):
◦ Necrose no local de injeção
Desconhecido (a frequência não pode ser estimada com os dados disponíveis):
◦ Alterações no eletrocardiograma (intervalo QT prolongado)
◦ Inflamação dos pulmões, doença pulmonar
◦ A hipertensão intracraniana idiopática (aumento da pressão intracraniana à volta do cérebro caracterizada por dor de cabeça, visão dupla e outros sintomas visuais e tinido ou zunido em um ou em ambos os ouvidos)
◦ Manchas avermelhadas, não elevadas, semelhantes a um alvo ou circulares no tronco, muitas vezes com bolhas centrais, descamação da pele, úlceras na boca, garganta, nariz, órgãos genitais e olhos. Estas erupções graves da pele podem ser precedidas por febre e sintomas semelhantes aos da gripe (síndrome de Stevens-Johnson/necrólise epidérmica tóxica).
◦ Vermelhidão da pele e erupção da pele com comichão (erupção tóxica da pele)
◦ Uma reação ada pele que causa manchas ou pontos vermelhos na pele, que podem parecer assemelhar-se a um alvo com um centro vermelho escuro circundado por anéis de um vermelho mais pálido (Eritema Multiforme)
Outros efeitos indesejáveis:
Outros efeitos indesejáveis que têm sido descritos na literatura com ligação ao tratamento com leuprorrelina, a substância ativa do ELIGARD, são o edema (acumulação de fluídos nos tecidos, manifestando-se com o inchaço das mãos e dos pés), embolia pulmonar (resultando em sintomas como falta de ar, dificuldade em respirar e dor no peito), palpitações (consciência do bater do coração), fraqueza muscular, arrepios, erupção na pele, memória debilitada e visão debilitada. Um aumento dos sinais de diminuição da densidade óssea (osteoporose) pode ser esperado após um tratamento de longa duração com ELIGARD. Devido à osteoporose, o risco de fraturas aumenta.
Foram raramente relatadas reações alérgicas graves, que causam dificuldade em respirar ou tonturas, após a administração de medicamento da mesma classe de ELIGARD.
Foram reportadas convulsões após a administração de medicamentos da mesma classe de ELIGARD.
Comunicação de efeitos indesejáveis:
Se tiver quaisquer efeitos indesejáveis, incluindo possíveis efeitos indesejáveis não indicados neste folheto, fale com o seu médico, farmacêutico ou enfermeiro. Também poderá comunicar efeitos indesejáveis diretamente através do sistema nacional de notificação mencionado abaixo. Ao comunicar efeitos indesejáveis, estará a ajudar a fornecer mais informações sobre a segurança deste medicamento.
Sítio da internet: http://www.infarmed.pt/web/infarmed/submissaoram (preferencialmente) ou através dos seguintes contactos:
Direção de Gestão do Risco de Medicamentos
Parque da Saúde de Lisboa, Av. Brasil 53
1749-004 Lisboa
Tel: +351 21 798 73 73
Linha do Medicamento: 800222444 (gratuita)
E-mail: farmacovigilancia@infarmed.pt
5. Como conservar ELIGARD
Manter este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após o prazo de validade impresso na embalagem exterior, após EXP. O prazo de validade corresponde ao último dia do mês indicado.
Instruções de conservação:
Conservar no frigorífico (2ºC - 8ºC).
Conservar na embalagem de origem para proteger da humidade.
Este produto deve ser armazenado à temperatura ambiente antes da injeção. Retire do frigorífico, aproximadamente 30 minutos antes da utilização. Uma vez fora do frigorífico este produto deverá ser armazenado na embalagem original à temperatura ambiente (inferior a 25ºC) até quatro semanas.
Após a abertura do estojo, o medicamento deve ser preparado e administrado imediatamente. Apenas para utilização única.
Instruções para eliminação das embalagens de ELIGARD não usadas ou expiradas:
Não deite fora quaisquer medicamentos na canalização ou no lixo doméstico. Pergunte ao seu farmacêutico como deitar fora os medicamentos que já não utiliza. Estas medidas irão ajudar a proteger o ambiente.
6. Conteúdo da embalagem e outras informações
Qual a composição de ELIGARD:
A substância ativa é o acetato de leuprorrelina.
Uma seringa pré-cheia (Seringa B) contém 22,5 mg de acetato de leuprorrelina.
Os outros componentes são Poli (ácido DL-láctico-co-glicólico) (75:25) e N-Metil2- pirrolidona na seringa pré-cheia com solução para injeção (Seringa A).
Qual o aspeto de ELIGARD e conteúdo da embalagem:
ELIGARD é um pó e solvente para solução injetável. ELIGARD 22,5 mg está disponível nas seguintes apresentações:
• Uma embalagem termomoldada e uma agulha estéril de 20-gauge dentro de uma embalagem de cartão. O estojo contém uma bolsa dessecante e um sistema de seringas pré- conectadas que consiste em:
◦ seringa A pré-cheia com solvente
◦ seringa B pré-cheia com pó
◦ conector com um botão de travão para a seringa A e B
• uma embalagem contendo 2 kits de um sistema de seringas pré-conectadas. É possível que não sejam comercializadas todas as apresentações.
Titular da Autorização de Introdução no Mercado e Fabricante:
Titular da Autorização de Introdução no Mercado:
RECORDATI Indústria Chimica e Farmacêutica S.p.A.
Via Matteo Civitali, 1
20148 Milão
Itália
Fabricante:
RECORDATI Indústria Chimica e Farmacêutica S.p.A.
Via Matteo Civitali, 1
20148 Milão
Itália
Este medicamento está autorizado nos Estados Membros do EEE com os seguintes nomes:
Áustria: Eligard Depot 22,5 mg
Bélgica: Depo-Eligard 22,5 mg
Chipre: Eligard República
Checa: Eligard
Dinamarca: Eligard
Estónia: Eligard
Finlândia: Eligard
França: Eligard 22,5 mg
Alemanha: Eligard 22,5 mg
Hungria: Eligard 22,5 mg
Islândia: Eligard
Irlanda: Eligard 22,5 mg
Itália: Eligard
Letónia: Eligard 22,5 mg
Lituânia: Eligard 22,5 mg
Luxemburgo: Depo-Eligard 22,5 mg
Países Baixos: Eligard 22,5 mg
Noruega: Eligard
Polónia: Eligard 22,5 mg
Portugal: Eligard 22,5 mg
Eslováquia: Eligard 22,5 mg
Eslovénia: Eligard 22,5 mg
Espanha: Eligard Trimestral 22,5 mg
Suécia: Eligard
7. Informação para os profissionais de saúde
A informação que se segue destina-se apenas aos profissionais de saúde:
Espere que o medicamento atinja a temperatura ambiente, retirando-o do frigorífico aproximadamente 30 minutos antes da utilização.
Por favor, prepare primeiro o doente para a injeção, seguindo-se a preparação do medicamento de acordo com as instruções abaixo indicadas. Se o produto não for preparado utilizando a técnica apropriada, este não deve ser administrado, uma vez que pode ocorrer falta de eficácia devido a uma incorreta reconstituição do produto.
Passo 1: Numa superfície limpa, abra estojo (rasgando a folha de alumínio a partir dos cantos para remover o seu conteúdo. Descarte o dessecante. Remova o sistema de seringa pré- conectado (Figura 1.1) do estojo. Abra a embalagem da agulha de segurança (Figura 1.2) retirando a aba de papel. Nota: A Seringa A e a Seringa B ainda não devem estar alinhadas.
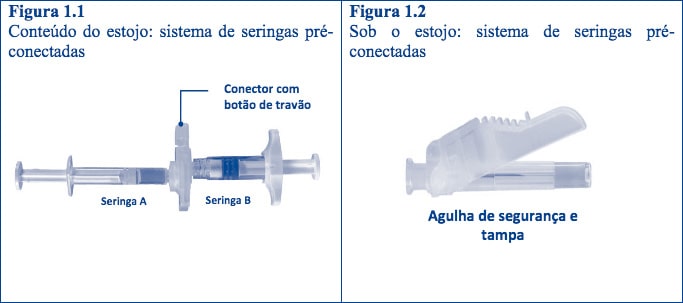
Passo 2: Segure o botão de travão no conector com o dedo e o polegar e pressione (Figura 2) até ouvir um som de estalo. As duas seringas serão alinhadas. Nenhuma orientação específica do sistema de seringas é necessária para ativar o conector. Não dobre o sistema de seringas (por favor, note que isto pode causar vazamento uma vez que pode parcialmente desapertar as seringas).
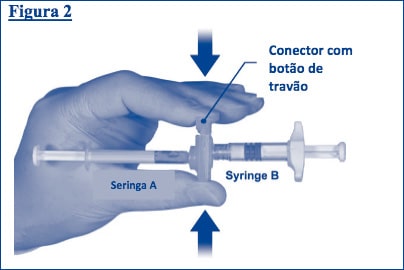
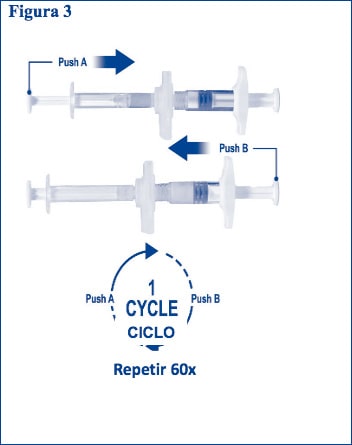
Passo 3: Segure as seringas numa posição horizontal, enquanto transfere o líquido da Seringa A para a Seringa B que contém o pó de acetato de leuprorrelina.
Misture cuidadosamente o produto durante 60 ciclos empurrando suavemente o conteúdo de ambas as seringas para a frente e para trás (um ciclo é um empurrão do êmbolo para a Seringas A e um empurrão do êmbolo para a Seringa B) (Figura 3). Não incline o sistema da seringa (por favor, note que isto pode causar vazamento uma vez que pode parcialmente desapertar as seringas).
Após perfeitamente misturada, a solução viscosa obterá uma cor no intervalo entre esbranquiçada a amarelo-pálido (que poderá incluir tonalidades entre o branco e o amarelo pálido).
Importante: Após o processo de mistura, prossiga imediatamente com o passo seguinte porque o produto fica mais viscoso ao longo do tempo. Não refrigere o produto misturado.
Por favor, note: o produto deve ser misturado conforme descrito, agitar NÃO IRÁ providenciar uma mistura adequada do produto.
Passo 4: Após misturar, mantenha as seringas verticalmente com a Seringa B por baixo. As seringas devem permanecer firmemente unidas. Transfira todo o conteúdo misturado para a Seringa B (seringa curta e larga) empurrando para baixo o êmbolo da Seringa A e retirando ligeiramente o êmbolo da Seringa B (Figura 4).
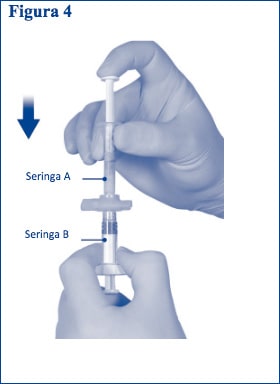
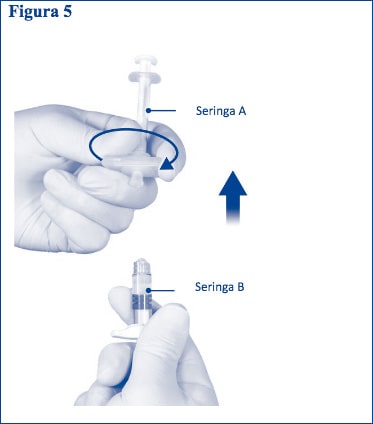
Passo 5: Enquanto se assegura que o êmbolo da Seringa A está a ser totalmente empurrado para baixo, segure o conector e desaparafuse-o da Seringa B. A Seringa A permanecerá presa ao conector (Figura 5). Assegure que não há perda de produto para que a agulha fique corretamente fixa aquando da sua colocação.
Por favor, note: uma grande ou algumas pequenas bolhas de ar podem permanecer na formulação, isto é aceitável.
Por favor, não remova as bolhas de ar da Seringa B, nesta fase o produto pode ser perdido!
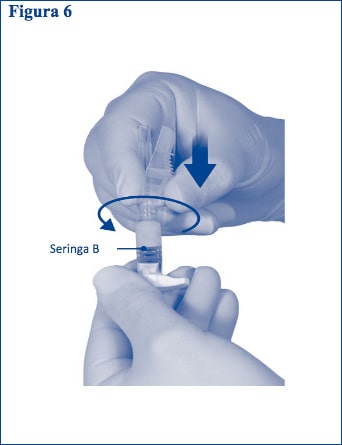
Passo 6:
• Segure a seringa B na posição vertical e mantenha o êmbolo branco para trás a fim de evitar perda do produto.
• Fixe a agulha de segurança na seringa B segurando a seringa e rodando cuidadosamente a agulha no sentido horário aproximadamente três quartos de volta até a agulha estar fixada (Figura 6).
Não aperte excessivamente, uma vez que isso pode causar fendas no encaixe da agulha, resultando no extravasamento do produto durante a injeção. A proteção de segurança também pode ser danificada se a agulha for aparafusada com muita força.
Se o encaixe da agulha rachar, parecer estar danificado ou apresentar alguma fuga, o produto não deve ser utilizado. A agulha danificada não deve ser substituída e o produto não deve ser injetado. Deve ser eliminada a totalidade do produto de forma segura.
Em caso de danos no encaixe da agulha, deve ser utilizado um novo produto de substituição.
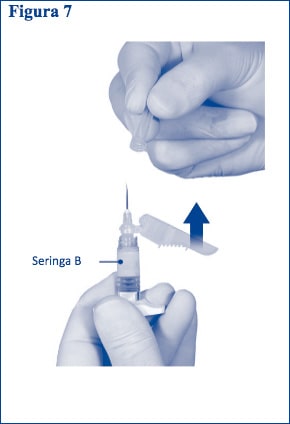
Passo 7: Afaste a proteção de segurança da agulha e puxe a cobertura de proteção da agulha imediatamente antes da administração (Figura 7).
Importante: Não efetue o mecanismo da agulha de segurança antes da administração. Caso o cubo da agulha pareça estar danificado ou a vazar, o produto NÃO deve ser usado. A agulha danificada NÃO deve ser substituída e o produto NÃO deve ser injetado. Em caso de danos no cubo da agulha, use outro kit ELIGARD.
Passo 8: Antes da administração, purgue todas as bolhas de ar grandes da Seringa B. Administre o produto por via subcutânea, mantendo a proteção de segurança afastada da agulha.
Procedimento de Administração:
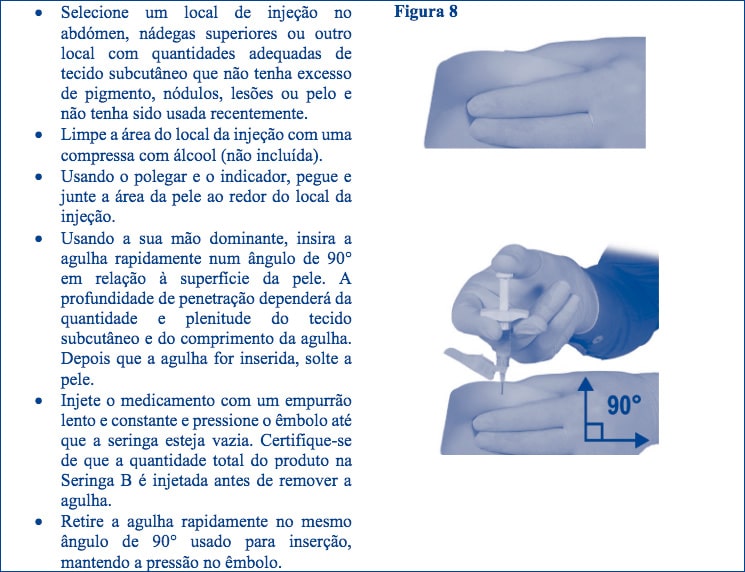
Passo 9: Após a injeção, bloqueie a proteção de segurança, utilizando qualquer um dos métodos de ativação abaixo.
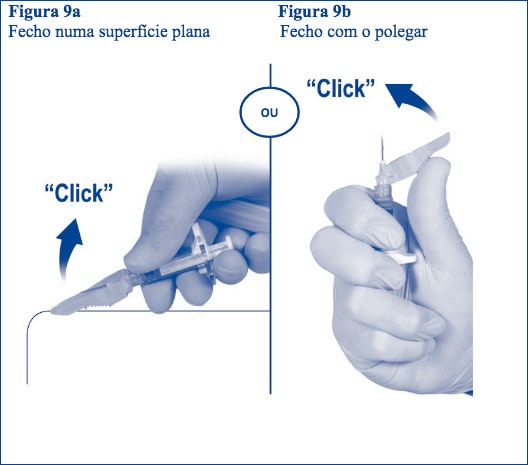
1. Encerramento numa superfície plana.
Pressione a proteção de segurança, do lado da alavanca para baixo, sobre uma superfície plana (Figura 9a) para cobrir a agulha e bloquear a proteção.
Verifique a posição de bloqueio com o “clique audível e tátil. A posição de bloqueio irá cobrir completamente a ponta da seringa.
2. Encerramento com o polegar
Coloque o polegar sobre a proteção de segurança (figura 9b), cubra a agulha e bloqueie a proteção.
Verifique a posição de bloqueio com o “clique audível e tátil. A posição de bloqueio irá cobrir completamente a ponta da seringa.
Uma vez bloqueada a proteção de segurança, coloque de imediato a agulha e a seringa num contentor apropriado.