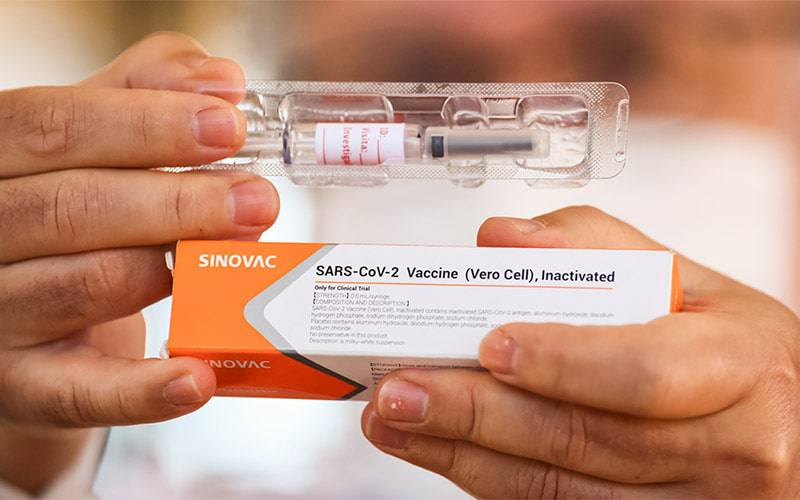
COVID-19: EMA avança com revisão da vacina inativada da Sinovac
O Comité de Medicamentos de Uso Humano (CHMP) da Agência Europeia de Medicamentos (EMA) anunciou o início da revisão contínua da Vacina COVID-19 (Célula vero) Inativada, desenvolvida pela Sinovac Life Sciences Co., Ltd.
SOCIEDADE E SAÚDE
NOVO COVID-19, FAQ – PERGUNTAS MAIS FREQUENTES
COVID-19, PERGUNTAS MAIS FREQUENTES LER MAIS
A decisão do CHMP de iniciar a revisão contínua baseia-se em resultados preliminares de estudos laboratoriais (dados não clínicos) e estudos clínicos. Estes estudos sugerem que a vacina desencadeia a produção de anticorpos que visam o SARS-CoV-2, o vírus que causa a COVID-19, e pode ajudar a proteger contra a doença.
A EMA explica que esta revisão “continuará até que haja provas suficientes para um pedido formal de autorização de introdução no mercado”.
A EMA avaliará a conformidade da vacina COVID-19 (Célula Vero) Inativada com as normas habituais da UE em matéria de eficácia, segurança e qualidade. Embora não possa prever os prazos globais, “deve levar menos tempo do que o normal para avaliar uma eventual aplicação devido ao trabalho realizado durante a revisão em curso”, esclarece a EMA numa nota de imprensa.
A vacina contra a COVID-19 (Célula vero) Inativada deverá preparar o organismo para se defender contra a infeção por SARS-CoV-2. A vacina contém SARS-CoV-2 que foi inativado (morto) e não pode causar a doença. Esta vacina, explica a EMA, “também contém um adjuvante, uma substância que ajuda a fortalecer a resposta imune”.
“Quando uma pessoa recebe a vacina, o seu sistema imunitário identifica o vírus inativado como estranho e produz anticorpos contra este. Se, mais tarde, a pessoa vacinada entrar em contacto com o SARS-CoV-2, o sistema imunitário reconhecerá o vírus e estará pronto para defender o corpo contra este”, acrescenta.